《化学能与热能》典例精析一
【例1】对下列化学反应现象,不正确的说法是( )
①放热的反应发生时不必加热
②化学反应一定有能量变化
③一般地,吸热反应需要加热后才能发生
④化学反应热效应数值与参加反应物质多少有关
A.①② B.②③ C.①③ D.②④
【解析】放热反应有许多是需要加热的,如碳燃烧;吸热反应有的不加热也能进行,如Ba(OH)2·8H2O与NH4Cl晶体反应。
【答案】C
【例2】某反应过程中能量变化如下图,则该反应的ΔH值为( )
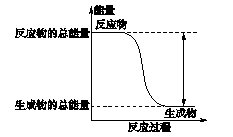
A.ΔH>0 B.ΔH<0 C.ΔH=0 D.无法判断
【解析】根据图示可知:反应物的总能量高于生成物的总能量,该反应是放热反应,故ΔH<0。
【答案】B
【例3】下列关于反应热的叙述正确的是( )
A.当ΔH<0时,表示该反应为吸热反应
B.由C(s)+1/2O2(g)=CO(g)的反应热为110.5 kJ·mol-1,可知碳的燃烧热为110.5 kJ·mol-1
C.反应热的大小与反应物所具有的能量和生成物所具有的能量无关
D.1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应放出的热量:CH3COOH<HNO3
【解析】ΔH<0时,表示该反应为放热反应;燃烧热应是在101 kPa下,1 mol可燃物完全燃烧生成稳定的氧化物所放出的热量,碳的燃烧热应为1 mol C完全燃烧生成CO2时所放出的热量;当反应物的总能量大于生成物的总能量时,反应放热,反之则吸热;由于CH3COOH为弱电解质,弱电解质的电离要吸热,所以D选项正确。
【答案】D
| 很有帮助 | 一点没用 | 马虎还行 | 点错路过 | 继续努力 |
- 上一篇:《化学能与电能》本节课本插图11幅
- 下一篇:《化学能与热能》典例精析二
相关文章
-
没有相关内容


 会员登录
会员登录