《无机非金属材料的主角——硅》典例精析二
1.下列物质的变化,不能通过一步化学反应完成的是( )
A.CO2→H2CO3 B.SiO2→Na2SiO3
C.Na2O2→Na2CO3 D.SiO2→H2SiO3
【解析】由于SiO2不溶水也不与水反应,所以由SiO2制取H2SiO3需先使SiO2与强碱反应制得可溶性硅酸盐后,再与酸反应才能制得H2SiO3。
【答案】D
2.能证明硅酸的酸性弱于碳酸酸性的实验事实是( )
A.CO2溶于水形成碳酸,SiO2难溶于水
B.CO2通入可溶性硅酸盐中析出硅酸沉淀
C.高温下SiO2与碳酸盐反应生成CO2
D.CO2是气体,而SiO2是固体
【解析】根据较强酸制较弱酸的原理,向可溶性硅酸盐溶液中通入CO2生成硅酸,可证明H2CO3酸性强于硅酸。
【答案】B
3.证明生石灰中既混有石英,又混有石灰石的正确方法是( )
A.加入过量的盐酸,观察是否有气泡冒出
B.加入过量的烧碱溶液,观察是否有固体溶解
C.加热至高温,观察是否有气泡冒出,是否有硅酸钙生成
D.先加过量的盐酸搅拌,观察是否有不溶物剩余及气泡出现;若有不溶物则滤出,投入到氢氧化钠溶液中看其是否溶解
【解析】SiO2不溶于除氢氟酸以外的任何酸,CaO、CaCO3均可溶于盐酸且CaCO3溶于盐酸有气泡生成,SiO2可以溶于NaOH溶液。
【答案】D
4.将过量的CO2分别通入①CaCl2溶液;②Na2SiO3溶液;③NaAlO2溶液;④饱和Na2CO3溶液;⑤Ca(OH)2,最终溶液中有白色沉淀析出的是( )
A.①②③④⑤ B.②③④
C.②④⑤ D.①②④
【解析】过量CO2通入Na2SiO3、NaAlO2有白色沉淀H2SiO3、Al(OH)3产生;过量CO2通入饱和Na2CO3溶液中:Na2CO3+CO2+H2O=2NaHCO3↓,生成的NaHCO3溶解度比Na2CO3溶解度小而结晶析出;过量的CO2通入Ca(OH)2溶液中最终生成Ca(HCO3)2而无沉淀析出:Ca(OH)2+2CO2=Ca(HCO3)2。
【答案】B
5.下列不属于硅酸盐产品的是( )
A.陶瓷 B.水泥 C.玻璃 D.光导纤维
【解析】陶瓷、水泥、玻璃都是传统的硅酸盐产品,光导纤维的主要成分是SiO2。
【答案】D
6.下列关于碳和硅的比较,正确的是( )
A.它们的最高价氧化物都能与水反应生成对应的酸
B.碳和硅的最高正价都是+4价
C.硅元素在地壳中的含量占第二位,碳占第一位
D.碳和硅在自然界存在形式都是既有游离态也有化合态
【解析】SiO2不溶于水也不与水反应,A不正确;在地壳中含量第一的是氧元素,硅占第二位,C不正确;自然界中有游离态的碳(金刚石),但是没有游离态的硅,因为硅是一种亲氧元素,D不正确。
【答案】B
7.下列有关硅及其化合物的说法正确的是( )
A.晶体硅具有金属光泽,可以导电,属于金属材料
B.常温下,硅的化学性质稳定,所以自然界中的硅大部分以游离态存在
C.SiO2是一种酸性氧化物,能够与水反应生成相应的酸
D.除去SiO2中混有的CaCO3可加入适量的稀盐酸
【解析】A项,晶体硅属于非金属单质;B项,硅具有亲氧性,自然界中主要以二氧化硅和硅酸盐的形式存在;C项,SiO2不与水反应;D项,SiO2不溶于稀盐酸,可使用稀盐酸除去其中混有的CaCO3。
【答案】D
8.几种含硅元素的物质之间的相互转化关系如图所示:

(1)写出图示反应的几种物质的化学式:
A ,B ,C ,D ,E 。
(2)写出下列反应的化学方程式:
①B→A: ;
②B→E: 。
(3)写出下列溶液中反应的离子方程式:
①A→D ;
②D→C 。
【解析】本题的突破点在于A和B,含硅的物质与碳在加强热的条件下反应的只有SiO2,其反应为![]() ,故A为Si,B为SiO2,则由硅的化合物之间关系可推知:C为H2SiO3,D为Na2SiO3,E为CaSiO3。
,故A为Si,B为SiO2,则由硅的化合物之间关系可推知:C为H2SiO3,D为Na2SiO3,E为CaSiO3。
【答案】(1)Si SiO2 H2SiO3 Na2SiO3 CaSiO3
(2)![]()
![]()
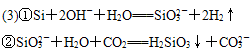
| 很有帮助 | 一点没用 | 马虎还行 | 点错路过 | 继续努力 |
- 上一篇:《无机非金属材料的主角——硅》典例精析一
- 下一篇:二氧化碳与二氧化硅的比较
相关文章
-
没有相关内容


 会员登录
会员登录