《溶解度》典例精析一
第一课时
【例题1】室温下,向一定质量的氯化钠溶液中加入10 g 氯化钠固体,充分搅拌后,尚有部分固体未溶解,加入10 g水后,固体全部溶解。下列判断正确的是( )
A.加水后一定是不饱和溶液 B.加水前可能是饱和溶液
C.加水后一定是饱和溶液 D.加水前一定是饱和溶液
【难度】中
【精析】本题考查的是理解饱和、不饱和溶液的含义。加水前,该溶液一定是饱和溶液,因为有固体剩余;加水后固体全部溶解,有可能是饱和溶液了,也有可能是不饱和溶液。
【答案】D
【例题2】室温时,有两瓶硝酸钾溶液,一瓶为饱和溶液(溶质的质量分数为40%),另一瓶为10%的溶液。下列实验操作中,无法区分这两种溶液的是( )
A.加一定量的水 B.加入少量硝酸钾晶体
C.略降低温度 D.室温时,蒸发少量水
【难度】中
【精析】本题考查的是饱和溶液与不饱和溶液的区别。饱和硝酸钾溶液继续加硝酸钾晶体无法溶解,降温或蒸发水份都会有晶体析出;而不饱和硝酸钾溶液无此现象。
【答案】A
【例题3】下列叙述中正确的是( )
A.饱和溶液降温析出晶体后的溶液仍为饱和溶液
B.饱和溶液的质量比不饱和溶液的质量大
C.一定温度时,某物质的浓溶液一定是饱和溶液
D.一定温度下,一定量溶剂中,饱和溶液不能溶解任何溶质
【难度】中
【精析】当某饱和溶液降温析出晶体后,该溶液一定不能继续溶解相应的溶质,因此它一定是饱和溶液,故A正确。饱和溶液与不饱和溶液的根本区别就在于能否继续溶解相应的溶质,与溶液质量的大小、溶液中含有溶质的多少无关,故B、C错误;某物质的饱和溶液只是不能继续溶解该物质,故D错误。
【答案】A
【例题4】将一杯20℃时的硝酸钾饱和溶液变为不饱和溶液,可采用的方法是( )
A.加入硝酸钾 B.升高温度 C.降低温度 D.蒸发溶剂
【难度】中
【精析】本题考查的是饱和溶液与不饱和溶液的相互转化。当温度升高时,在一定量的溶剂里,硝酸钾溶解的量会增大,因此,升高温度可使饱和硝酸钾溶液变成不饱和溶液。
【答案】B
【例题5】某学生在一定温度下,进行溶解硝酸钾的实验,记录的数据如下:
实验序号 | 1 | 2 | 3 | 4 |
所用水的质量/g | 100 | 100 | 100 | 100 |
加入KNO3的质量/g | 80 | 100 | 120 | 140 |
所得溶液的质量/g | 180 | 200 | 210 |
|
(1)根据上述数据分析,实验1得到的溶液是_________(填“饱和”或“不饱和”,下同)溶液,实验2得到的溶液是________溶液,实验3得到的溶液是________溶液。
(2)该温度下100g水中最多溶解KNO3的质量是__________。
(3)请你推测第4次实验时所得溶液的质量是__________。
【难度】中
【精析】根据表中数据可以看出,第1、2次实验所加入的硝酸钾均全部溶解,而第3次实验加入的120g硝酸钾只溶解了210g-100g=110g,说明在该温度下100g水中最多溶解110g硝酸钾,此时溶液已处于饱和状态,所以在第4次加入140g硝酸钾时,也只能溶解110g,所得溶液质量仍为110g+100g=210g。
【答案】(1)不饱和;不饱和;饱和;(2)110g;(3)210g
第二课时
【例题1】已知20℃时,氯化钠的溶解度为36g。
(1)20℃时,饱和氯化钠溶液中,溶质、溶剂与溶液的质量比为__________。
(2)若要配制20℃时的饱和溶液68g,则需氯化钠________,水________。
【难度】中
【精析】本题考查对固体溶解度含义的理解。“20℃时,氯化钠的溶解度为36g”这句话的含义为在20℃时,100g水中最多溶解36g氯化钠。而对于一定温度下的某物质的饱和溶液来说,它所含的溶质、溶剂与溶液三者之间的质量比是固定的,与溶液的多少无关。据此可进行求算。
【答案】(1)36:100:136 (2)18g 50g
【例题2】已知在101kPa时,M、N两种气体在不同温度下的溶解度数值:S(M,20℃)=0.023L/LH2O,S(N,40℃)=0.023L/LH2O 。则在101kPa、30℃时,M、N两种气体溶解度大小关系正确的是( )
A.S(M)<S(N) B.S(M)=S(N) C.S(M) >S(N) D.无法比较
【难度】中
【精析】气体溶解度随温度的升高而减小,故M在30℃时的溶解度小于0.023;N在30℃时的溶解度大于0.023。
【答案】A
【例题3】一定温度下,向下图所示烧杯中加入一定量水,仅有部分晶体溶解。所得溶液与原溶液相比,说法正确的是( )
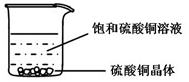
A.溶剂的质量增加,溶液颜色变浅
B.溶质溶解度不变,溶液颜色变深
C.溶质的质量增加,溶液颜色变深
D.溶质溶解度不变,溶液颜色不变
【难度】中
【精析】本是考查了固体溶解度的影响因素及溶液状态的判断。由于温度不变,所以溶质的溶解度不变;加入一定量水后仅有部分晶体溶解,所得溶液中溶质、溶剂质量都增加且溶液仍为该温度时的饱和溶液,所以溶液的颜色不变。
【答案】D
【例题4】甲、乙两种固体的溶解度曲线如图所示。下列叙述正确的是 ( )
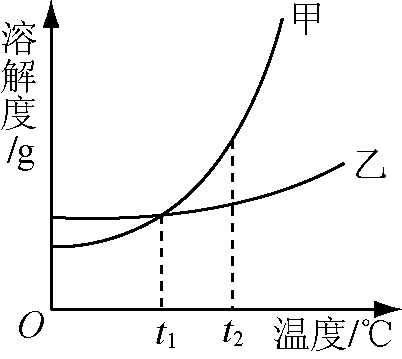
A.依据溶解度曲线可判断,甲的溶解度比乙的大
B.将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大
C.将t2℃时甲的饱和溶液变为不饱和溶液,可采取降温的方法
D.t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等
【难度】中
【精析】本题考查了溶解度曲线知识的应用。比较物质溶解度大小要指明温度,故A错误;甲的溶解度受温度变化影响较大,而乙的溶解度受温度变化影响较小,所以将等质量的甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大,如果溶液质量不相等,则难以判断,故B错误;甲的溶解度随温度的升高而增大,所以不能通过降低温度的方法将饱和溶液变为不饱和溶液,故C错误;t1℃时,甲和乙的溶解度相等,所以该温度下甲和乙的饱和溶液各100g,其溶质的质量一定相等,故D正确。
【答案】D
【例题5】根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
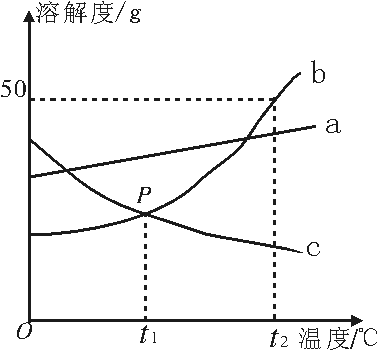
(1) 时,b、c两种物质的溶解度相等;
(2)t2℃时,将等质量的a、b、c加水溶解配制成饱和溶液,所得溶液的质量由大到小为 ;
(3)把b物质的不饱和溶液变为饱和溶液,下列有关说法正确的是 (填序号);
A.溶剂的质量一定变小
B.溶质的质量可能不变[
C.溶质的质量一定变大
D.该饱和溶液还可以溶解其它物质
(4)t2℃时,50 g b物质加入到50 g水中充分溶解后,所得溶液的质量为 ;
(5)b中含有少量的a,若要提纯b,可采用 结晶的方法。
【难度】难
【精析】本题考查了溶解度曲线知识的应用。(1)曲线的交点表示该温度时两物质的溶解度相等;(2)溶解度越小,等质量溶质形成饱和溶液所需水的量越多,所以形成溶液的质量c>a>b ;(3)温度越高,b物质的溶解度越大,把b物质的不饱和溶液变为饱和溶液的方法有三种:加b物质、蒸发溶剂或降温。而降温法溶液中溶质、溶剂、溶液的质量都不变,故B正确;而饱和的b溶液只是该温度时不能继续溶解b物质,还能溶解其它物质,故D也正确; (4)t2℃时,b物质的溶解度为50g,所以50g水最多只能溶解25g b物质;(5)b的溶解度受温度影响变化较大,而a的溶解度受温度影响变化不大,所以用降温结晶法。
【答案】(1)t1 ℃(2)c>a>b (3)BD (4)75g(5) 降温(或冷却热饱和溶液)
| 很有帮助 | 一点没用 | 马虎还行 | 点错路过 | 继续努力 |
- 上一篇:《溶解度》知识全解
- 下一篇:《溶解度》典例精析二
相关文章
-
没有相关内容


 会员登录
会员登录