铜与浓硫酸的反应实验要点
1.实验原理:
![]()
2.实验装置:
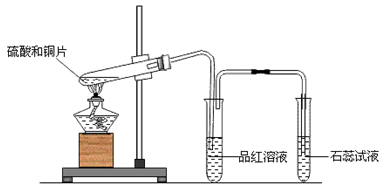
3.实验仪器及药品:
铁架台、分液漏斗、圆底烧瓶、酒精灯、试管、铜片、浓硫酸、品红溶液。
4.
实验步骤 | 实验现象 | 实验结论及化学方程式 |
①按上图所示将仪器组装好,检验装置的气密性,并按要求加入各种试剂,观察铜片在浓硫酸中的现象 | 加热前,铜片在浓硫酸中无现象产生 | 常温下,铜与浓硫酸不反应 |
②点燃酒精灯,加热试管,同时观察试管中的现象 | 加热后,试管中的品红溶液逐渐变为无色,石蕊试液变红 | 在加热条件下,铜与浓硫酸反应,生成二氧化硫 |
③冷却后,向试管中注入蒸馏水,观察溶液的颜色 | 圆底烧瓶中的溶液呈蓝色 | 反应方程式为:
|
5.注意事项:
(1)加热时,试管外壁要擦干,要先预热。否则试管一旦炸裂,浓硫酸洒落,必将酿成严重的事故。
(2)该实验中的铜片不能用铁片或铝片代替,其原因是Fe、Al遇浓硫酸钝化,Fe、Al表面生成一层致密氧化膜而阻止反应进一步进行。与金属反应时,浓硫酸既显氧化性,又显酸的性质。随着反应的进行,硫酸浓度变小,一旦变为稀硫酸,反应就会停止。
| 很有帮助 | 一点没用 | 马虎还行 | 点错路过 | 继续努力 |
- 上一篇:浓、稀硫酸的鉴别
- 下一篇:演示实验4-7《二氧化硫与水的反应》高清…
相关文章
-
没有相关内容


 会员登录
会员登录