《溶液的形成》典例精析三
【例1】将白醋、食用油、食盐、酒精分别放入水中,不能形成溶液的是( )
A.白醋 B.食用油 C.食盐 D.酒精
【解析】直接选择法:解析这四种物质及我们实际生活的经验,不难得出白醋、食盐、酒精都能溶解于水,形成均一、稳定的混合物,而食用油与水混合,静置后会分层,形成不均一、不稳定的混合物,不能形成溶液。
【答案】B
【提示】对溶液概念的理解。
【例2】下列关于溶液的叙述,正确的是( )
A.凡是均一的、稳定的、澄清、透明的液体一定是溶液
B.一杯溶液上部分溶质少,下部分溶质多
C.溶液只要外界条件不变,不论放置多长时间,溶质都不会从溶剂中分离出来
D.NaOH溶液加入到硫酸铜溶液中恰好完全反应,溶质是NaOH,溶剂是CuSO4
【解析】错选A是溶液概念不清,认为均一、稳定、透明的液体就是溶液;错选D是因为认为NaOH溶液加入到 CuSO4溶液中,NaOH溶液是被溶解的,CuSO4溶液是溶解NaOH溶液的。
正确答案:C
【例3】把少量下列物质分别放入水中,充分搅拌后可以得到溶液的是( )
A.植物油 B.面粉 C.硫酸锌 D.硫酸铜
【解析】本题考查溶液的概念。将植物油放到水中搅拌、静置,将出现分层现象,不具备均一性和稳定性,不属于溶液;将面粉放到水中搅拌、静置,面粉沉入水底,不符合溶液的基本特征,不是溶液;硫酸锌和硫酸铜放到水中搅拌、静置,不发生任何变化,符合溶液的基本特征,属于溶液。
【答案】C D
【例4】具有下列性质的物质中,一定是溶液的是( )
A.澄清、透明、稳定、均一的液体
B.澄清的石灰水中通人少量二氧化碳后所形成的液体
C.过量的锌粒加入稀硫酸中反应后过滤所得到的液体
D.温室下将5 g大理石加入100 g水中搅拌所得的物质
【解析】A中所述液体可能是纯净物而不是混合物,如乙醇、蒸馏水等,故A错;CO2+Ca(OH)2=CaCO3↓+H2O,形成的液体中有不溶于水的CaCO3,故B错;C中形成的是ZnSO4溶液,故C正确。D中大理石不与水反应,也不溶于水,故D错。
【答案】C
【例5】指出下列各种溶液中的溶质和溶剂。
A.75%的酒精溶液 B.稀盐酸 C.澄清的石灰水
D.碘酒 E.硫酸铜溶液 F.锌和稀硫酸恰好完全反应后所形成的溶液
【解析】本题中所考查的都是一些典型的溶液。题中稀盐酸的溶质易错答为盐酸,而盐酸本身就是HCl气体的水溶液;碘酒的溶剂易答为“酒”,而“酒”本身就是酒精的水溶液;硫酸铜溶液中溶质易错答成铜,溶质易错答成硫酸,没有考虑到硫酸铜本身就是一种物质,溶质即为硫酸铜,溶剂是水。
【答案】
溶液 | A | B | C | D | E | F |
溶质 | 酒精 | HCl气体 | Ca(OH)2 | 碘 | CuSO4 | ZnSO4 |
溶剂 | 水 | 水 | 水 | 酒精 | 水 | 水 |
【例6】病人在医院接受静脉注射或滴注时,常用生理盐水即氯化钠注射液。如图是某药业公司生产的氯化钠注射液包装标签上的部分文字。请回答:

(1)该注射液里的溶质是_________________;
(2)常温下,一瓶合格的氯化钠注射液液封放置一段时间后,是否会出现浑浊现象?为什么?
【解析】溶液的特点:均一、稳定。若外部条件不改变,溶液不论放置多长时间,溶质也不会从溶液中分离析出。
【答案】(1)氯化钠 (2)不会。在常温、密封放置的情况下,该氯化钠溶液是稳定的。
【例7】一种“即食即热型快餐”适合外出旅行时使用。其内层是用铝箔包裹的并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质混合,即可对食物进行加热,这两包化学物质最合适的选择是( )
A.浓硫酸与水 B.生石灰与水 C.熟石灰与水 D.氯化钠与水
【解析】此题是以一种“即食即热型快餐”为素材设计的一道信息题,这样的命题立意较好地体现了当今的素质教育的要求和新课程的理念,推进探究学习,使学生感受化学就在我们身边,拉近化学与学生的距离,使学生感受化学学习的乐趣,化学为我们所用,教育学生在平常的学习、生活中要多观察、多思考、多解析,点评化学现象的适应范围。此题目在知识与技能上是对哪些物质溶解于水时溶液温度升高及化学反应伴随的发热现象的考查。A、B、D三个选项都有物质溶解于水的情况,C、D中食盐和熟石灰是学生生活中常见的物质,凭生活经验便知溶解时溶液温度无明显变化;A在课堂探究实验中便知浓硫酸溶于水时,溶液温度升高,学生通过各种媒体对浓硫酸有强腐蚀性已具备感性认识,加上浓硫酸又是液体不便贮存,所以A不太合适;生石灰与水混合时发生化学反应,生成熟石灰,同时放出大量的热量,加上“旺旺雪饼”等一些食品包装内都用生石灰作干燥剂,同学们由于好奇肯定对干燥剂“生石灰”做过各种探究,对它是块状固体,腐蚀性不太大,遇水放热等知识的认识深刻,通过比较可以确认B最适合。
【答案】B
【例8】某同学设计如图所示的装置,分别向两个烧杯中加入适量的水,A烧杯中加入NH4NO3固体,B烧杯中加入NaOH固体,小心搅拌。待固体完全溶解后,拿起两只烧杯,将发生什么现象?试简要地解析产生上述现象的原因。
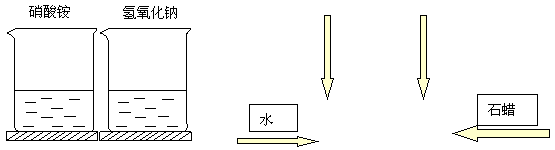
你还能设计出几种方案(方案可直接用实验简图表示)?可供选择的某些用品有:NaCl、NaOH、NH4NO3、浓硫酸……(你还可选用其他一些仪器和药品)。
【解析】探究物质溶解时的热效应的方案设计,应围绕温度的变化考虑,如用手触摸杯壁、用温度计测定、利用温度改变使冰融化或石蜡熔化或使水结冰、使密闭容器内气体的体积膨胀等。
【答案】A烧杯底部与木块凝结在一起,B烧杯底部与木块分离。A烧杯中硝酸铵溶解于水,溶液温度降低,使水凝结成冰;而B烧杯中氢氧化钠溶解于水,溶液温度升高,使石蜡熔化。
溶解过程中放热与吸热的现象:
物质 | 原因(填“<”“>”或“=”) | 温度 |
NaOH | 扩散吸收的热量<水合放出的热量 | 升温 |
NH4NO3 | 扩散吸收的热量>水合放出的热量 | 降温 |
NaCl | 扩散吸收的热量=水合放出的热量 | 温度无明显变化 |
方案一:可将试管中水加热至沸腾后,撤掉酒精灯,然后加入氢氧化钠固体,试管内水立即沸腾;
方案二:在试管中溶解,立即塞上带导管的单孔橡皮塞,同时将导管的另一端放入盛水的水槽(或装有水的U形管)中,观察导管口是否有气泡放出(或U形管内水面的变化)。(其他合理答案均可)
| 很有帮助 | 一点没用 | 马虎还行 | 点错路过 | 继续努力 |
- 上一篇:《溶液的形成》典例精析二
- 下一篇:九年级化学精编导学练9.1《溶液的形成》
相关文章
-
没有相关内容


 会员登录
会员登录