《利用化学方程式的简单计算》典例精析一
【例1】氢化锂(LiH)为玻璃状无色透明固体,军事上用作氢气发生来源,反应的化学方程式为:LiH+H2O=LiOH+H2↑。计算80 g氢化锂与足量的水反应生成氢气的质量。
【精析】该题是已知反应物氢化锂的质量求生成物氢气的质量,所以根据两者的质量比等于相对分子质量之比进行列比例式可求得。
【答案】解:设生成氢气的质量为x。
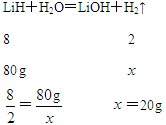
答:可生成的氢气的质量为20 g。
【例2】锌与稀硫酸反应生成硫酸锌和氢气,反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑。制取标准状况下的氢气2.24 L,至少需要多少克锌与足量的稀硫酸反应,同时能产生多少克硫酸锌?(标准状况下氢气的密度为0.09 g/L)
【精析】本题是已知生成物的体积,求反应物及另一生成物的质量,计算时先要将2.24 L氢气换算成质量,且单位要统一,然后根据物质间的固定质量比即可求出。
【答案】解:反应生成氢气的质量为0.09 g/ L×2.24 L=0.2 g
设至少需要锌的质量为x,同时能产生硫酸锌的质量为y。
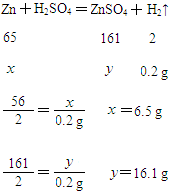
答:至少需要6.5 g锌,同时生成16.1 g硫酸锌。
| 很有帮助 | 一点没用 | 马虎还行 | 点错路过 | 继续努力 |
相关文章
-
没有相关内容


 会员登录
会员登录