实验室制取二氧化碳析疑
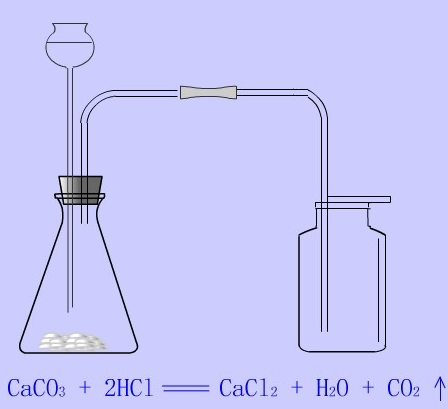
1.为什么选用大理石或石灰石制取二氧化碳?
大理石或石灰石的主要成分是碳酸钙。碳酸盐跟酸起反应,一般都有二氧化碳生成。若选用可溶性的碳酸盐(如碳酸钠等),与酸反应速度过快,难以控制;若选用其他不溶性碳酸盐(如碳酸镁等),其来源一般又较少。大理石或石灰石与酸反应速度适中,在自然界里含量也极其丰富,价格低廉。所以,选用大理石或石灰石制二氧化碳。
2.实验室制取二氧化碳时,为什么最好选用稀盐酸?
如果用稀硫酸和大理石或石灰石反应,结果生成微溶性固体硫酸钙,它覆盖在大理石或石灰石表面,使酸与大理石或石灰石脱离接触,导致反应太缓慢。
如果用硝酸与大理石或石灰石反应,由于硝酸是一种不稳定性的酸,在见光或受热时易分解,从而使制得的CO2中混有NO2和O2等杂质。
如果用浓盐酸和大理石或石灰石反应,由于浓盐酸具有挥发性,使制得的CO2中混有较多的氯化氢气体。
用稀盐酸和大理石或石灰石反应,所得CO2气流平稳,气体又较为纯净,所以选用稀盐酸制CO2最合适。
3.实验室制取二氧化碳的装置,需要哪些仪器?使用时应注意什么事项?
仪器有广口瓶(或平底烧瓶、锥形瓶等)、长颈漏斗、双孔橡皮塞、导管、集气瓶。
使用时应注意的事项有:
(1)要用镊子夹取石灰石或大理石。装入广口瓶(或平底烧瓶、锥形瓶等)时要注意“一横、二放、三竖”。
(2)插入气体发生装置内的导管只需刚刚露出塞子即可,这样才能有利于气体导出。
(3)稀盐酸应从长颈漏斗加入,长颈漏斗的下端管口要伸入液面以下,防止反应生成的气体从长颈漏斗逸出。
(4)不能用酒精灯加热制CO2。
4.怎样证明生成的气体是二氧化碳?
把产生的气体通入盛有澄清石灰水的试管中,若石灰水变浑浊,则证明生成的气体是CO2。
5.用什么方法收集二氧化碳?
CO2能溶于水,故不能用排水法收集;CO2的密度比空气大,故采用向上排空气法收集CO2。
6.怎样检验集气瓶里是否充满了二氧化碳?
用一根燃着的木条放在集气瓶口,若木条立即熄灭,则证明瓶内已充满CO2,否则说明CO2没有收集满。
7.实验室里能否用启普发生器来制取二氧化碳?
能。用启普发生器来制取的气体必须符合以下三个条件:
(1)块状固体和液体反应产生气体;
(2)生成的气体难溶于水;
(3)反应不需加热。
实验室制取CO2常用块状的大理石或石灰石与稀盐酸反应,且反应不需加热,生成的CO2气体虽能溶于水,却难溶于稀盐酸。所以,能用启普发生器来制取CO2。
| 很有帮助 | 一点没用 | 马虎还行 | 点错路过 | 继续努力 |
相关文章
-
没有相关内容


 会员登录
会员登录