《糖类》知识全解
课标要求
1.掌握糖类的主要代表物:葡萄糖、蔗糖的组成和重要性质,它们之间的相互转变以及与烃的衍生物的关系。
2.能举例说明糖类在食品加工和生物质能源开发上的应用。
重难点突破
本节课的教学重点:掌握糖类重要的代表物葡萄糖、蔗糖的组成和重要性质,它们之间的相互转变以及与烃的衍生物的关系。
突破方法:是用探究实验来证明葡萄糖和蔗糖的重要性质,再通过课堂讨论,引导学生对比、分析、比较葡萄糖与蔗糖的结构与性质的关系。
本节课的教学难点:糖类的概念、葡萄糖的结构和性质。
突破方法:通过科学探究,使学生主动思考,自主设计实验,探究葡萄糖的性质,并由此来推测出葡萄糖所具有的结构和性质。
教法建议
在化学必修2中已经了解了糖类的具体物质与分类,学习了葡萄糖的分子式,在实验的基础上认识了它的还原性,如:与银氨溶液的反应及与新制氢氧化铜悬浊液的反应,但没有进一步书写反应的化学方程式,也没有通过实验推断它的结构。本课开篇引导学生回忆一下已有的知识,再利用醛基、羟基的性质等已有的知识内容,结合探究性实验,进行演绎、推理、探测葡萄糖的结构。根据结构分析葡萄糖的化学性质,再由性质结合生活实际分析葡萄糖的应用。加深了学生对葡萄糖的认识,提升了学生的分析、推理、知识迁移能力以及科学的探究精神。通过对糖类在实际生活中的应用的了解,认识化学物质对人类社会的重要意义。
学法建议
在课前自主预习时,学生应复习一下必修2《基本营养物质》一章中学到的有关单糖、二糖、多糖的概念,以及葡萄糖、蔗糖的结构和性质的相关知识。本节课的内容与原来的这些知识联系的比较紧密,有了好一点的基础后学习本节课程也会相对容易一些。运用类推、迁移的方法掌握糖类主要代表物的性质,通过探究实验,完成知识的建构。经过学习小组间的合作探究,使学生再次体会到实验是学习和研究物质化学性质的重要方法。通过单糖、双糖、多糖的探究实验,可以进一步体验对化学物质的探究过程,理解科学探究的意义,学会科学探究的基本方法,提高科学探究的能力,体验科学探究大的乐趣。
知识集合
1.糖类的组成和结构
(1)组成:含有碳、氢、氧三种元素。
(2)结构:从分子结构上看,糖类可定义为多羟基醛、多羟基酮和它们的脱水缩合物。
(3)分类
| 单糖 | 二糖 | 多糖 |
能否水解 | 不能 | 能 | 能 |
代表物质 | 葡萄糖、果糖、核糖及脱氧核糖 | 麦芽糖、乳糖、蔗糖 | 淀粉、纤维素 |
2.葡萄糖和果糖
(1)组成与结构
| 葡萄糖 | 果糖 |
分子式 | C6H12O6 | C6H12O6 |
结构简式 | CH2OH(CHOH)4CHO |
|
官能团 | —OH和 | —OH和 |
相互关系 | 互为同分异构体 | |
(2)葡萄糖的化学性质及用途
①化学性质

②用途:葡萄糖用于制镜业、糖果制造业、医药业,为体弱和低血糖患者补充营养。
3.蔗糖和麦芽糖
| 蔗糖 | 麦芽糖 | |
分子式 | C12H22O11 | C12H22O11 | |
结构特点 | 分子中没有醛基 | 分子中有醛基 | |
化学性质 | 相似点 | 水解反应
| 水解反应
|
不同点 | 不能被银氨溶液或新制氢氧化铜悬浊液氧化 | 能被银氨溶液或新制的氢氧化铜悬浊液氧化 | |
相互关系 | 互为同分异构体 | ||
4.淀粉和纤维素
(1)淀粉
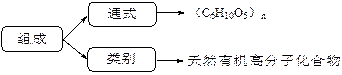
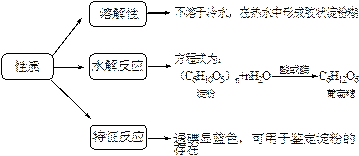
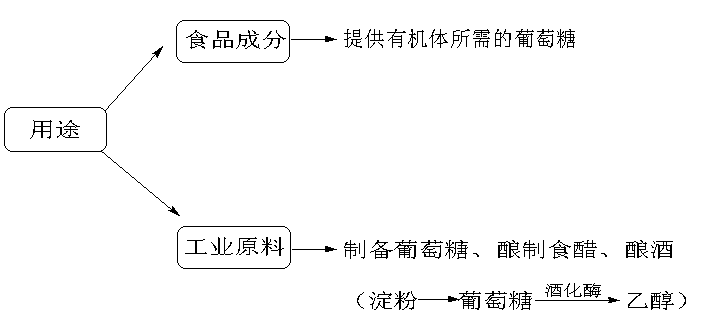
(2)纤维素
①组成:通式为(C6H10O5)n,属于天然有机高分子化合物。
②性质:
a.溶解性:一般不溶于水和有机溶剂。
b.水解反应:
![]()
c.酯化反应:纤维素的葡萄糖单元中含有羟基,可与含氧酸发生酯化反应。
③用途:
纤维素可以用于纺织工业、造纸业等。纤维素酯化后的产物可用于制造塑料、油漆等。
5.淀粉水解程度的检验
(1)实验原理
①淀粉遇碘显蓝色,但不发生银镜反应。
②葡萄糖:遇碘不显蓝色,但可以发生银镜反应。
(2)实验步骤
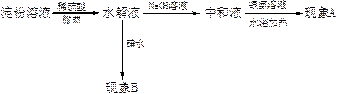
(3)实验现象及结论
| 现象A | 现象B | 结论 |
① | 未出现银镜 | 溶液变蓝色 | 淀粉尚未溶解 |
② | 出现银镜 | 溶液变蓝色 | 淀粉部分溶解 |
③ | 出现银镜 | 溶液不变蓝色 | 淀粉完全溶解 |
| 很有帮助 | 一点没用 | 马虎还行 | 点错路过 | 继续努力 |
- 上一篇:《油脂》知识全解
- 下一篇:选修5课堂达标验收练习4.1《油脂》
相关文章
-
没有相关内容


 会员登录
会员登录