《有机化合物的结构特点》知识全解
课标要求
1.认识有机化合物的成键特点。
2.了解有机化合物的同分异构现象。
3.掌握同分异构体的书写方法。
重难点突破
本节课的教学重点是:有机物的成键特点,同分异构现象。
突破方法:从学生最熟悉的有机物—烷烃入手,利用球棍模型,实物展示,引导学生总结出碳原子的成键特点,从而进一步归纳出有机化合物的结构特点及同分异构现象。
本节课的教学难点是:有机化合物的同分异构体的书写。
突破方法:引导学生认识到同分异构体书写方法的重要性,在课堂上准备出充分的练习时间,让学生在课堂上熟练掌握同分异构体的书写方法和注意事项。并进行适当的扩展,初步学会书写除烷烃外的其他官能团有机物的同分异构体,并在练习的基础上给学生归纳常见的官能团异构情况。
教法建议
高中化学课程改革的基本思路强调形成积极主动的学习态度,倡导学生主动参与、乐于探究、勤于动手,培养学生搜集和处理信息的能力、获取新知识的能力、分析和解决问题的能力以及交流与合作的能力。本节教学中采用了“自学──引导”式教学方法,通过引导学生做好课前预习培养学生的自学、发现问题的能力。
共价键的形成与分子结构是从微观上揭示物质构成的奥秘,较为抽象。由于学生在化学2模块与“物质结构与性质”模块中均已初步认识,本节的教学要充分利用学生已有的知识,调动学生主动探索科学规律的积极性。通过烷烃分子模型的制作,引导学生分析模型的共同点和不同点,最后找出共性和个性之间的联系。
同分异构体的书写是学生的一个学习难点。因此课堂上引导学生注意书写的方法很重要,要预留足够的练习时间。对于同分异构体的书写,还要适当地进行扩展,初步学会书写除烷烃外的其他单官能团有机物的同分异构体,在练习的基础上给学生归纳常见的官能团异构情况。
学法建议
有机化合物的分子结构多为空间立体构型,所以为了能更清晰的理解有机物的空间构型,学生可以自己制作常见有机物的球棍模型,把书本上的二维视觉转化成三维视觉,切身体会有机分子的立体结构。并在教师引导下自己归纳出碳原子成键方式与空间构型的关系。从而认识有机化合物的立体异构。
知识集合
一、碳原子的成键特点
1.碳原子价键为四个
2.碳原子间的成键方式:C-C、C=C、C≡C
3.碳原子间的结合方式:既可以结合成碳链,还可以结合成碳环
4.共价键的三个参数
(1)键长:成键的2个原子,原子核间的距离称为键长,一般说来,键长越短,键越牢固。
(2)键能:以共价键结合的双原子分子,裂解成原子时所吸收的能量称为键能,键能越大,键越牢固。
(3)键角:分子中1个原子与另外2个原子形成的两个共价键在空间的夹角,决定了分子的空间构型。
二、有机物组成与结构的表示方法
1.化学式:C2H6
2.最简式(实验式):CH3
3.电子式: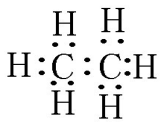
4.结构式: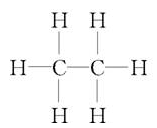
5.结构简式:CH3CH3
三、烷烃的结构特征:
1.甲烷具有正四面体的结构特征,烷烃中的碳原子都采取sp3杂化。
2.当烷烃中的碳原子数大于3的时候,碳链就形成锯齿形状。
3.烷烃中的碳氢键和碳碳键都是σ键。
4.同系物:结构相似、分子组成上相差一个或若干个CH2原子团的物质互相称为同系物。
四、有机化合物的同分异构现象
1.同分异构体现象:化合物具有相同的分子式,但具有不同结构的现象
同分异构体:具有相同的分子式,但具有不同结构的化合物互称为同分异构体
三个相同:分子组成相同、相对分子质量相同、分子式相同
二个不同:结构不同、性质不同
2.同分异构体常见三种类型
(1)碳链异构(如丁烷与异丁烷)
(2)官能团位置异构(如1-丁烯与2-丁烯)
(3)官能团种类异构(如乙醇与甲醚)
3.同分异构体的书写
碳链由长到短;支链由整到散;位置由里到边;排布由邻到间。
| 很有帮助 | 一点没用 | 马虎还行 | 点错路过 | 继续努力 |
- 上一篇:《有机化合物的分类》知识全解
- 下一篇:《有机化合物的命名》知识全解
相关文章
-
没有相关内容


 会员登录
会员登录